Je voudrais initier aujourd’hui une série d’articles qui auront pour but de vous exposer mes travaux dans la recherche scientifique et de rendre le tout intelligible aux visiteurs curieux sans être forcément spécialistes. Pour ce premier billet, je vais vous parler des travaux que nous avons publiés en décembre 2015 sur la flavobactériose. Avant d’en parler, je pose d’abord le contexte de travail.
Passage de la biologie végétale à l’ichtyopathologie
Depuis 2012, j’ai eu l’occasion de changer de thématique de recherche et de passer de la biotechnologie végétale et l’amélioration des qualités du fruit à la microbiologie animale, l’ichtyopathologie (ou étude des maladies des poissons). Étant donné que je me suis très rapidement spécialisé en biologie végétale lors de ma formation initiale et que j’avais alors toujours travaillé sur la laitue, le tabac mais finalement surtout sur la tomate, pour ceux qui me connaissent, cette reconversion semblait assez surprenante pour ne pas dire contre-nature.
Thème apparemment diamétralement opposé mais pas tant que ça : certes je suis « végétaliste » mais surtout biologiste moléculaire et la biologie moléculaire, ça se pratique à peu près de la même manière si on travaille sur la tomate, les virus, les bactéries, l’homme ou le pangolin. J’aurais même tendance à dire que c’est un poil plus compliqué de travailler sur les plantes et qu’extraire des acides nucléiques de truite quand on a extrait de l’ARN de feuille de fraisier, c’est aussi difficile que de se reconvertir en vigile d’une boite dans une bourgade du Massachusetts après avoir fait la guerre du Vietnam : on a tendance à sortir aussitôt l’artillerie lourde au moindre pépin alors qu’en fin de compte, il suffit de faire acte de présence pour être efficace.
Accueilli au département « Nutrition Santé et Filières Agricoles » de Bordeaux Sciences Agro
 J’ai donc été accueilli à Gradignan, près de Bordeaux, dans un laboratoire de Bordeaux Sciences Agro, l’école nationale supérieur des sciences agronomiques de Bordeaux Aquitaine, anciennement appelée ENITA, tout simplement l’école d’ingénieurs agronomes de la région. Plus particulièrement dans une équipe du département « Nutrition-Santé et Filières Agricoles » (NSFA) dirigé par Hervé Jacob. Ce département regroupe plusieurs équipes d’enseignants-chercheurs qui travaillent sur des thèmes très variés : les probiotiques utilisables en santé humaine comme en agriculture (élevage comme cultures végétales !), la nutrition humaine, la qualité de la viande et le bien-être animal au sens large (juste avant qu’il ne passe à la casserole, entendons nous bien…). Malheureusement, même s’il y a un espace consacré sur le site de l’école, le département NSFA n’a pas de site internet digne de ce nom qui permette d’englober d’un seul regard l’ensemble des activités de recherche. C’est bien dommage.
J’ai donc été accueilli à Gradignan, près de Bordeaux, dans un laboratoire de Bordeaux Sciences Agro, l’école nationale supérieur des sciences agronomiques de Bordeaux Aquitaine, anciennement appelée ENITA, tout simplement l’école d’ingénieurs agronomes de la région. Plus particulièrement dans une équipe du département « Nutrition-Santé et Filières Agricoles » (NSFA) dirigé par Hervé Jacob. Ce département regroupe plusieurs équipes d’enseignants-chercheurs qui travaillent sur des thèmes très variés : les probiotiques utilisables en santé humaine comme en agriculture (élevage comme cultures végétales !), la nutrition humaine, la qualité de la viande et le bien-être animal au sens large (juste avant qu’il ne passe à la casserole, entendons nous bien…). Malheureusement, même s’il y a un espace consacré sur le site de l’école, le département NSFA n’a pas de site internet digne de ce nom qui permette d’englober d’un seul regard l’ensemble des activités de recherche. C’est bien dommage.
J’ai intégré la petite équipe dirigée par Michel Le Hénaff, maître de conférence spécialisé dans la microbiologie, et composée alors de Sandrine Papillon, ingénieur d’études spécialisée en chimie, et d’Alexandra Grasteau qui était doctorante (thèse soutenue en décembre 2015). Ma mission était alors d’intégrer un projet sur la lutte contre la flavobactériose.
Le problème de la flavobactériose dans les élevages de truites (et autres salmonidés)
Qu’est-ce que la flavobactériose ? C’est le nom générique d’une maladie bactérienne qui touche certains poissons, d’élevage ou sauvages. Le terme manque d’ailleurs de précision puisqu’il y a plusieurs espèces de flavobactéries qui touchent des gammes différentes de poissons sous la poussée de stress et conditions environnementales différentes. Je ne me suis occupé que d’une seule de ces espèces : Flavobacterium psychrophilum. « Flavo » signifie « jaune » (parce que ces bactéries synthétisent un pigment jaune, la riboflavine, facilement repérable quand on les met en culture) ; « psychro » signifie « froid » et « philum » signifie « qui aime ». La bactérie jaune qui aime le froid. Cette bactérie découverte au milieu du XXe siècle s’avère être à l’origine de deux maladies affectant principalement les salmonidés (saumons, truites, ombles, etc.) :

la première est la maladie des eaux froides (Bacterial Cold Water Disease, BCWD) qui affecte les poissons adultes et induit l’apparition d’ulcérations cutanées qui sont mortelles ou du moins rendent le poisson invendable. Cette maladie a commencé à poser problème en Amérique du Nord dans les années 1980, chez les salmonidés sauvages dont la progéniture (les œufs) était récupérée pour être exploitée dans la filière de l’alimentation ou pour le repeuplement de cours d’eau. Du fait de l’essor de la pisciculture et de la mondialisation (qui a entrainé l’exportation d’œufs et de poissons de l’autre côté de l’Atlantique et du Pacifique) la bactérie s’est invitée sur le Vieux Continent et dans ces pays asiatiques au climat tempéré où ces poissons sont consommés. Là, en Europe, une nouvelle forme de flavobactériose s’est exprimée dans les élevages de truites arc-en-ciel (et de truites fario) : le syndrome de l’alevin de la truite arc-en-ciel (Rainbow Trout Fry Syndrome, RTFS). Comme son nom l’indique cette maladie touche plutôt les jeunes poissons, les alevins. La maladie infecte de manière systémique ce jeune poisson dont les défenses immunitaires sont trop faibles pour être efficaces ; malade, celui-ci arrête de s’alimenter et meurt. Si le problème n’est pas pris à bras le corps par le pisciculteur, les pertes peuvent être importantes (on parle de cas où 90 % du banc de poissons est affecté).
Que ce soit la BCWD ou le RTFS, une seule espèce bactérienne responsable : Flavobacterium psychrophilum. Cette dernière est une espèce que l’on retrouve dans les cours d’eau avec d’autres espèces du même genre. Opportuniste, il semble qu’elle ne devienne problématique que lorsque des facteurs de stress se mettent en place chez le poisson : stress de manipulation, blessures, densité d’élevage trop importante, qualité d’eau de bassin médiocre ou variations de température, etc. Comme son nom l’indique, les crises de flavobactériose ont plutôt lieu quand les températures sont basses (avec un optimum autour de 15 °C).
Le soin consistant à donner un antibiotique mélangé à l’alimentation (le florfénicol, analogue du chloramphénicol plus connu des biologistes moléculaires), il est difficile pour les pisciculteurs de soigner les poissons malades puisque ces derniers ne s’alimentent plus. L’alimentation supplémentée ne sert alors qu’à protéger le reste du banc contre une infection provenant des poissons voisins ou des eaux de bassin. Cette solution n’est pas la panacée : tout d’abord elle est chère pour des animaux qui ne le sont pas mais surtout, l’usage des antibiotiques est controversé. Ces derniers doivent être utilisés le moins possible pour nos animaux comme pour nos rhumes, une sur-utilisation entrainera l’apparition de souches bactériennes antibiorésistantes et ce sera d’autant plus gênant que F. psychrophilum n’est sensible qu’au seul florfénicol. C’est le dernier carton de munitions, il vaut mieux ajuster le tir comme un sniper que faire un tir de barrage à la sulfateuse…
Le talent des pisciculteurs pour sauver leurs exploitations de ce fléau est de combiner tout un arsenal de mesures de prévention : mesures d’hygiène, nettoyages de bassins, désinfection des eaux en amont, traitements biocides prophylactiques réguliers. Les consommateurs n’ont pas idée du trésor de technicité qu’il faut développer pour obtenir cette truite-portion ou ce filet de saumon fumé qu’ils prennent nonchalamment à leur rayon poissonnerie préféré.

Mais la partie n’est pas encore gagnée, loin de là : la maladie progresse malgré les mesures de prévention déployées. Celle-ci n’est pas encore suffisamment connue : quels sont les réservoirs (c’est-à-dire les espèces ou compartiments écologiques où la bactérie demeure avant d’infecter les poissons) ? Quelle est la dynamique d’infection (cette question en sous-entendant deux autres que sont : quels sont les moyens de défense des poissons et comment sont-ils contournés ?) Quels moyens de prévention spécifique peut-on déployer (vaccins ? traitements biocides optimisés ?) Y a-t-il une marge d’optimisation pour les moyens de prévention non-spécifiques à F. psychrophilum ? Ou pour les pratiques d’élevage, l’utilisation de produits prébiotiques ou probiotiques ? Ajoutons à ça qu’il y a besoin d’outils de détection, de quantification de la bactérie, que ce soit pour la recherche et le développement des stratégies de prévention ou tout simplement assurer une traçabilité de leur efficience une fois qu’elles sont mises en place sur le terrain. Il y a déjà plein de méthodes de suivi de la flavobactériose mais il y a toujours une marge d’optimisation et/ou l’émergence de besoins spécifiques auxquels les outils existants ne permettent pas toujours de répondre.
C’est donc pour répondre à certaines de ces questions qu’un projet de recherche a été concocté. En partie financé par des fonds européens (le Fonds Européen de DEveloppement Régional, FEDER), la Région Aquitaine et le Comité Interprofessionnel des Produits de l’Aquaculture (CIPA), il a impliqué l’équipe de Michel Le Hénaff, le laboratoire départemental des Pyrénées et des Landes (LDPL, plus connu jadis comme le Laboratoire Départementale des Landes, LD40) représenté par Patrick Daniel et le Groupement de Défense Sanitaire Aquacole d’Aquitaine (GDSAA, pas de site internet… seriously ? Même pas un compte Twitter pour communiquer ?) représenté par Valérie Chesneau. Et bien entendu, un panel de pisciculteurs de la région Aquitaine-Limousin-Poitou-Charentes.
Réduire la transmission verticale de la Flavobactériose par l’optimisation des techniques de désinfection des œufs
C’est ce volet du projet « Flavo » que je vais aborder particulièrement dans ce billet déjà bien entamé. Il y en a eu d’autres mais celui-ci a fait l’objet d’une publication dans la revue Journal of Aquaculture Research and Development :
« Evaluation of Glutaraldehyde, Chloramine-T, Bronopol, Incimaxx Aquatic® and Hydrogen Peroxide as Biocides against Flavobacterium psychrophilum for Sanitization of Rainbow Trout Eyed Eggs » Auteurs : Alexandra Grasteau, Thomas Guiraud, Patrick Daniel, Ségolène Calvez, Valérie Chesneau et Michel Le Hénaff. Le PDF peut être téléchargé là.
Comme le veut l’usage, cet article est donc rédigé en anglais avec tous les détails techniques nécessaires pour reproduire les expériences en question et pour convaincre les lecteurs des conclusions que nous proposons. Rappelez vous que mon but ici n’est pas de vous en restituer le détail et encore moins de vous le traduire. Les spécialistes du domaine iront directement lire l’article et y trouveront tout ce dont ils ont besoin. Moi, ici, je veux vous en tirer les grandes lignes, souligner ce que je pense être les apports de notre travail et d’éventuelles perspectives. Je voudrais aussi préciser que je ne me fais en aucun cas le porte-parole de mes co-auteurs ni des institutions pré-citées. Considérez tout ceci comme une discussion autour d’un verre ou d’un café lors de laquelle vous me demanderiez ce sur quoi j’ai travaillé ces dernières années ou, en l’occurrence, sur quoi porte ma dernière publication.
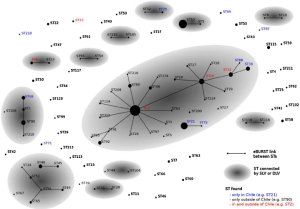
Image tirée de l’article de Avendaño-Herrera et al., Veterinary Microbiology, 2014
Revenons à la flavobactériose. Cette maladie est transmise de deux manières : la transmission horizontale c’est-à-dire par contact d’un individu à un autre, directement ou en contaminant l’environnement notamment l’eau de bassin, les sédiments, etc. (par analogie avec les humains, ce peut être une bise, un éternuement, une poignée de porte contaminée, etc.) et la transmission verticale c’est-à-dire la transmission d’un géniteur à sa progéniture (par comparaison, chez l’homme, ça correspondrait à la transmission du HIV de la mère à l’enfant). La propagation internationale de cette maladie a pu se réaliser à cause de la capacité de F. psychrophilum à se transmettre de manière verticale : Prélevés sur un lieu A, les œufs d’un géniteur infecté ont été utilisés pour l’élevage qui s’est réalisé en un lieu B, contaminant les autres poissons présents qui ont eux même donné une descendance infectée transférée à un lieu C, etc. La mobilité des poissons (naturelle ou via l’activité humaine) et l’alternance de la transmission verticale et horizontale ont permis la propagation de la maladie dans l’ensemble des pays producteurs de salmonidés. L’étude de l’évolution de certains gènes de Flavobacterium psychrophilum (par une stratégie de Multi Locus Sequence Typing, MLST, parfois combinée à celle de Pulsed-Field Gel Electrophoresis, PFGE, qui sont deux techniques qui permettent de déterminer une sorte de code-barre génétique pour chaque individu étudié et par conséquent d’avoir un aperçu de la structure génétique d’une population. Les souches évolutivement proches partageant tout ou partie de leur profil génétique tel qu’il est déterminé par MLST ou par PFGE. Je développe à la demande dans les commentaires !) semble démontrer que F. psychrophilum s’est répandue de cette manière, de proche en proche, de géniteur à la progéniture, se partageant une souche qui évolue petit à petit. D’autres études sur la transmission verticale (du géniteur à l’œuf) montrent la réalité de cette hypothèse : la femelle adulte est porteuse saine (ses défenses immunitaires lui permettent d’y survivre) et les bactéries présentes dans sa cavité abdominale sont transmises aux ovules pendant la longue phase qui précède la ponte. Les bactéries survivent jusqu’à l’éclosion et infectent la jeune larve (le petit poisson obtenu après éclosion est appelé larve. Plus tard la larve deviendra alevin puis truitelle et truite adulte), l’épidémie se déclenchant ensuite localement lorsque les conditions deviennent favorables.
La flavobactériose n’étant pas la seule maladie transmise par les œufs, les pisciculteurs tentent déjà de prévenir la transmission verticale de diverses maladies, ceci par le biais d’étapes de désinfection des œufs et d’élimination manuelle des œufs affectés (qui peuvent par exemple changer de couleur quand ils meurent). Or ces mesures de prévention ne sont pas toutes adaptées à la flavobactériose. Tout d’abord, la présence de F. psychrophilum dans les œufs ne leur est pas nuisible : ils survivent et ne présentent pas de symptôme particulier qui permette de les repérer et les éliminer manuellement. Ensuite, les traitements désinfectants utilisés de nos jours ont pour la plupart été développés pour prévenir d’autres maladies (bactériennes, fongiques, virales ?). Celui qui est le plus utilisé est basé sur les propriétés désinfectantes de la povidone iodée ou des molécules analogues. Vous connaissez sûrement cette molécule puisque ce n’est rien d’autre que de la bétadine qui est en quelque sorte un grosse molécule polymère sur laquelle sont liées des molécules d’iode qui portent le pouvoir désinfectant et qui sont relarguées petit à petit dans le milieu ; sans ce système, le pouvoir désinfectant de l’iode serait trop fugace et instable. Malheureusement, les traitements actuels (en terme de concentration et en terme de temps de contact) ne sont pas suffisamment agressifs pour affecter durablement Flavobacterium psychrophilum et prévenir sa transmission à la progéniture salmonidée.
Durant nos travaux, nous avons porté notre attention sur d’autres molécules désinfectantes, une douzaine parmi les produits potentiellement utilisables par les pisciculteurs. Parmi eux, les plus marquants sont le florfénicol (l’antibiotique utilisé pour soigner les poissons) ou encore le chlorure de sodium (le sel de table, toxique pour F. psychrophilum… et pour la truite) mais surtout cinq molécules candidates comme le bronopol, le glutaraldéhyde, le peroxyde d’hydrogène, l’acide peracétique et la chloramine. Le choix s’est finalement porté sur ces molécules parce que leurs propriétés anti-flavobactériennes étaient mal cernées et/ou parce qu’elles étaient prometteuses (le peroxyde d’hydrogène et l’acide peracétique sont inoffensifs pour l’environnement, le glutaraldéhyde qui lui est potentiellement très toxique pour la bactérie).
Une des méthodes couramment utilisées pour déterminer le pouvoir désinfectant d’une molécule est la détermination de sa Concentration Minimale d’Inhibition (CMI) : ça consiste à ajouter une molécule candidate en concentration croissante dans une solution bactérienne et observer sa croissance. Si la culture bactérienne continue à croitre à telle concentration de désinfectant, c’est qu’elle n’est pas suffisamment concentrée ; si la culture bactérienne ne croit plus, la concentration de désinfectant est suffisante. La concentration de désinfectant la plus basse ayant le pouvoir de bloquer la croissance bactérienne détermine la CMI. Joli sur le papier mais cette méthode implique un temps de contact long, plusieurs jours, qui ne correspond pas à la réalité des traitements désinfectants opérés par les pisciculteurs (quelques minutes à une heure, les œufs ayant besoin d’un apport d’oxygène (O2), ils ne peuvent pas rester trop longtemps sans renouvellement de l’eau sans s’asphyxier). Certes, si un désinfectant est suffisamment concentré pour inhiber la croissance bactérienne sur plusieurs jours, on se doute que la population bactérienne est bel et bien détruite avant que la molécule désinfectante ne soit naturellement dégradée. Mais du fait de l’absence d’information concernant la rémanence du désinfectant et le temps de contact nécessaire pour détruire la population bactérienne, nous avons préféré proposer une autre méthode pour estimer le pouvoir anti-flavobactérien de notre panel de produits désinfectants.
Pour déterminer ce pouvoir bactéricide, nous avons utilisé une méthode basée sur les barèmes de stérilisation en génie industriel : on expose une population de F. psychrophilum à un désinfectant à une concentration donnée et on suit l’évolution de cette population au cours d’un temps limité et connu (jusqu’à 40 min en ce qui nous concerne, la fourchette haute des durées de désinfection que s’autorisent les pisciculteurs). Cette expérience nous donne pour chaque concentration le temps nécessaire pour décimer la population (réduire une population au 1/10ème de ce qu’elle était initialement), on appelle ça le temps de réduction décimale. Ceci nous permet de proposer un jeu de correspondances entre durée de traitement et concentration de désinfectant pour obtenir le même degré de destruction. On pourrait naturellement arguer que la décimation d’une population bactérienne est loin d’être une désinfection totale mais les chiffres que nous avons obtenus semblent indiquer que les intensités de traitements utilisées jusqu’alors en pisciculture étaient en deçà de ce qui est nécessaire pour ne serait-ce que décimer les populations de F. psychrophilum. Avant de déterminer les intensités de traitement nécessaires pour réduire une population de F. psychrophilum d’un facteur 100 ou 1000, il nous a paru plus pertinent de tester les différentes intensités de traitements sur la viabilité des œufs de truite.
Pour cela, nous avons fait une expérience très simple : pour chacun des désinfectants d’intérêt, nous nous sommes calés sur une durée de traitement de 20 minutes correspondant à ce qui est pratiqué sur le terrain et avons choisi trois concentrations différentes : une suboptimale proche de celle utilisée actuellement dans la filière, une concentration qui correspond aux intensités de traitement que nous avons précédemment déterminées et une concentration exagérément haute que nous pensions délétère pour les œufs de truite. Après traitement, nous avons laissé les œufs se développer et, après éclosion, attendu que les larves deviennent alevins et commencent à se nourrir. Le but du jeu étant de pouvoir observer d’éventuelles malformations.
Le résultat, c’est que les œufs de truite sont incroyablement résistants : ils ont bien entendu survécu aux traitements les plus faibles (déjà connus pour leur innocuité envers les œufs puisque utilisés dans la profession), aux nouvelles conditions de traitements mais aussi aux intensités de traitement les plus violentes. A un désinfectant près puisque les plus traitements les plus forts réalisés avec le glutaraldéhyde avaient quand même un impact négatif ; résultat à pondérer puisque je suspecte que l’efficacité du rinçage post-désinfection améliore la survie des œufs. S’il fallait perdre 10 % des œufs grâce à un traitement violent mais ponctuel pour réduire les traitements prophylactiques subséquents et la survenue de crises de flavobactériose, le jeu pourrait en valoir la chandelle, non ? Mais ça reste encore à prouver, ce n’est qu’une opinion personnelle. Toujours est-il que les autres désinfectants même très concentrés n’affectent pas la survie des œufs et n’entrainent ni malformation ni variation de poids (ce qui n’est pas indiqué dans l’article mais qui a quand été vérifié). Ce qui en soit est intéressant pour la profession qui sait maintenant qu’elle bénéficie d’une plus grande marge de manœuvre (technique à défaut d’être administrative…) pour ces traitements de désinfection avec notamment des substances inoffensives pour l’environnement comme le peroxyde d’hydrogène ou l’acide peracétique.
Les réalisations moins évidentes de ces travaux mais non moins intéressantes
Si les résultats principaux sont la mise au point de traitements anti-flavobactériens plus efficaces et inoffensifs pour les œufs et alevins subséquents, je voudrais maintenant mettre en avant trois points de ces recherches que je trouve intéressants.
- Le plus trivial c’est la réalisation de paniers d’incubation compartimentés. Ils n’ont pas été achetés quelque part mais bel et bien imaginés et réalisés par Michel Le Hénaff et Alain Rives de Bordeaux Sciences Agro. Basés sur les dimensions d’un modèle utilisé en pisciculture, ils assurent un débit optimal et peuvent contenir 200 œufs/larves dans chaque compartiment sachant que chaque panier d’incubation en contient six. Ce dispositif très pratique nous a permis de tester un nombre optimal de répétitions sur un espace réduit et surtout dans des conditions similaires : on a obtenu une meilleure reproductibilité sur une expérimentation en ferme aquacole sans occuper un espace excessif dans cette dite ferme. Ce qui n’est pas un vain mot quand on considère que les fermes piscicoles participantes l’ont fait bénévolement et sur la base du volontariat. Ce serait dommage qu’un tel dispositif ne profite pas au plus grand nombre sur d’autres types d’expérimentations.
- L’autre réalisation, c’est le test de viabilité par EMA-qPCR que nous avons mis au point pour suivre la survie de Flavobacterium psychrophilum exposée aux divers traitements biocides. Nous n’avons pas inventé la technique, loin de là, elle date au moins de 2006, mais la mise au point était ardue et je suis d’autant mieux placé pour en parler que c’est moi qui l’ai réalisée ainsi que les tests qui ont suivi. Cette technique fait appel au monoazide d’éthidium (EMA). Cette molécule est ce qu’on appelle un intercalant qui se fixe à l’ADN. Activé par une forte intensité lumineuse, il se fixe définitivement à l’ADN qu’il clive au passage. Si on combine cette propriété au fait que cette molécule ne pénètre pas dans les cellules saines, on peut l’utiliser pour distinguer les cellules mortes des cellules vivantes : si la cellule est vivante, l’EMA ne rentre pas dans la cellule, ne se fixe à rien et sa photo-activation n’a aucun impact, l’ADN de la cellule vivante demeure détectable une fois qu’on l’a extrait. Si la cellule est morte ou mourante, l’EMA rentre dans la cellule, se fixe à l’ADN et la photo-activation entraine la dégradation de l’ADN qu’on ne peut plus détecter par la suite. Nous avons utilisé les techniques bien connues de PCR qui permettent de détecter spécifiquement et de quantifier l’ADN de F. psychrophilum. On nous a reproché de ne pas avoir utilisé une méthode de quantification classique qui consiste à mettre les bactéries en culture et de les compter. D’autant plus que la technique sophistiquée que nous avons utilisée est plus chère. C’est un débat vieux de quinze ans désormais, les techniques d’énumération sont robustes et peu chères et, même si je suis biologiste moléculaire et plutôt enclin à utiliser des techniques toujours plus innovantes, je suis très sensible à ce genre d’argument. Mais concrètement, une fois la mise au point réalisée, cette technique d’EMA-qPCR permet de manipuler simultanément un grand nombre de petits échantillons dans les mêmes conditions et d’avoir les résultats pour un désinfectant dans la journée voire en une grosse demi-journée si on est rôdé. On peut potentiellement adapter le protocole pour quantifier la viabilité dans des cultures un peu particulières comme les biofilms dans lesquels la proportion de bactéries cultivables/non-cultivables n’est pas forcément idéale pour les techniques classiques d’énumération. Cette technique me semble prometteuse, le seul point noir est le besoin de mise au point spécifique à chaque espèce bactérienne testée. Mise au point déjà réalisée pour F. psychrophilum…
- Le dernier point intéressant de ces travaux outre les apports pour la filière piscicole, c’est l’utilisation de ces fameux barèmes de stérilisation, la détermination de ces temps de réduction décimale. C’est utilisé dans le milieu industriel pour la mise au point de méthodes de stérilisation par la chaleur par exemple. Ou pour l’enzymologie, la préservation des qualités nutritionnelles de produits alimentaires pendant leur transformation. Quelque chose de finalement assez exotique dans le milieu de l’ichtyopathologie : un article de revue est récemment sorti sur les diverses techniques et marges d’optimisation des techniques de désinfection des œufs et il n’en ressort pas que cette méthode d’objectivation des propriétés désinfectantes d’un produit soit particulièrement utilisée ni même connue. Au delà de ce jeu de correspondances Durée de traitement/Concentration de biocide utilisable pour les pisciculteurs, ce système nous donne accès à une autre valeur plutôt abstraite de prime abord mais non dénuée d’intérêt : la valeur Z aussi appelée paramètre de thermorésistance caractéristique d’un micro-organisme. Dans notre cas, on pourrait appeler cette valeur le paramètre de chimiorésistance caractéristique d’un micro-organisme (ou on pourrait continuer à l’appeler valeur Z, hein ?). Concrètement, cette valeur correspond à l’augmentation de concentration nécessaire pour réduire la durée d’exposition de 90 % ou pour être 10 fois plus efficace dans le pouvoir désinfectant. Exemple fictif, si on a une valeur Z de 100 g/L pour de la poudre de perlimpinpin qui détruit 90 % d’une suspension de levure en 40 min en l’utilisant à 200 g/L, ça veut dire que si on augmente cette concentration de 100 g/L (la valeur Z) en passant à 300 g/L, on détruit 90 % des levures en 4 min au lieu de 40 min ou on détruit 99 % des levures en 40 min au lieu de 90 %. A l’inverse, si on réduit la concentration de la poudre de perlimpinpin à 100 g/L, on sait qu’il va falloir 400 min (~7 h) pour éliminer 90 % des levures ou qu’en 40 min, on n’en aura éliminé que 9 %. Ce paramètre Z étant spécifique d’un biocide et d’un micro-organisme, il peut aussi être exploité de deux manières : pour un micro-organisme donné, il permet de comparer le pouvoir désinfectant de différentes molécules. Ainsi, dans l’article, on montre que l’Incimaxx (l’acide peracétique) est beaucoup plus agressif que le peroxyde d’hydrogène alors qu’ils fonctionnent tous les deux de la même manière sur la bactérie. Le corolaire, c’est que ça veut aussi dire que si on se plante un peu dans la confection de la solution de peroxyde d’hydrogène, ça aura moins d’impact qu’en manipulant de l’Incimaxx. L’autre utilisation de cette donnée, c’est plutôt pour la recherche : pour une molécule désinfectante donnée, on peut comparer la chimiorésistance de différents micro-organismes voire même plusieurs souches de la même espèce (par exemple une souche de F. psychrophilum isolée sur du saumon royal, une souche isolée sur de l’ayu, une autre sur de la truite arc-en-ciel, etc). Ça nous permettrait de phénotyper ces souches, c’est-à-dire décrire les caractéristiques spécifiques d’une souche. Comme pour le typage génétique (le génotypage) dont j’ai parlé plus haut (MLST/PFGE), ce genre d’informations sert à mieux comprendre l’évolution d’un organisme et son adaptation à son environnement et son hôte. Mieux comprendre le pathogène pour mieux lutter contre lui. Et tout ça, ces « barèmes de stérilisation », ça peut être utile pour d’autres maladies que la flavobactériose des poissons mais peut aussi être utilisé pour la santé humaine, l’agro-alimentaire, l’œnologie, les herbicides, etc. Voire toute étude visant à caractériser l’impact d’un facteur/traitement sur une population (ex: impact de l’installation d’un logiciel sur un parc informatique sur la prévalence de virus/spywares, comparaison de l’impact de campagnes de prévention sur la prévalence de fumeurs ou d’accidents de la route, etc.). On sort de mon domaine d’expertise, je suppose que des méthodes d’objectivation du même genre sont utilisées d’une manière ou d’une autre…
Concluons sur ce billet qui commence à être plus long que l’article originel. J’espère que j’ai atteint les objectifs principaux que je me suis fixé : raconter mon boulot à mon entourage plus ou moins proches (famille, amis, anciens collègues ou contacts divers) d’une manière suffisamment précise mais accessible au risque de produire un texte assez touffu mais sur lequel on peut revenir à loisir, visibiliser nos recherches (c’est-à-dire à la fois expliciter le contenu de mon CV et exposer les travaux de cette équipe de Bordeaux Sciences Agro) et porter un éclairage peut-être nouveau sur certains aspects de la pisciculture, ce à quoi les éleveurs peuvent être confrontés et comment la recherche peut répondre à certains de leurs besoins. Je voudrais préciser que ces travaux sont bel et bien de la recherche appliquée, ce sont des expériences préliminaires et non pas des pratiques industrielles du genre inonder les cours d’eau de France et de Navarre avec des hectolitres de glutaraldéhyde… Je précise une fois de plus que cet article n’est pas un publireportage de la filière aquacole ni même de Bordeaux Sciences Agro, c’est juste moi, Thomas Guiraud, qui devise sur des travaux de recherche déjà publiés.
A l’avenir, je souhaiterais faire le même type d’article sur mes précédents travaux (de thèse, de post-doc) avec une limitation, c’est que je ne peux pas aborder avec précision les travaux non publiés (et il y en a pas mal de 2005 à 2012). Je verrais le moment venu. Concernant la flavobactériose, le projet en question était plus large, il y a eu d’autres résultats qui sont en cours de valorisation ou qui ont servi à d’autres projets en cours. J’en parlerai sur le blog mais je ne peux pas aller plus vite que la musique…
PS : les images viendront petit à petit pour égayer ce pavé :3
